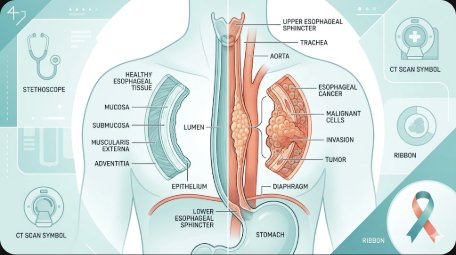
식도암이란? — 정의와 핵심 포인트
식도암(Esophageal Cancer)은 음식물이 인두에서 위까지 전달되는 관 모양 장기인 식도(esophagus)의 점막에서 발생하는 악성종양입니다. 2026년 국가암등록통계에 따르면 식도암은 한국인 전체 암 발생 중 약 2.1%를 차지하며, 남성에서 여성보다 약 8~10배 높은 발생률을 보입니다. 조기 발견 시 5년 생존율이 70% 이상까지 올라가지만, 상당수가 진행된 단계에서 발견되어 전체 5년 생존율은 약 15~25%에 머물러 있어 조기 검진과 위험인자 관리가 매우 중요합니다.
식도암은 크게 편평세포암(Squamous Cell Carcinoma, SCC)과 선암(Adenocarcinoma) 두 가지 조직학적 유형으로 나뉘며, 한국에서는 편평세포암이 전체의 약 90%를 차지합니다. 반면 서구에서는 역류성 식도염·바렛식도와 관련된 선암 비율이 꾸준히 증가하고 있어, 유형별 원인·치료 전략이 다릅니다.
식도암 초기 증상 — 놓치기 쉬운 7가지 신호
식도암은 초기에 자각 증상이 거의 없어 ‘침묵의 암’이라 불립니다. 다음 증상이 2주 이상 지속되면 반드시 전문의 진료를 받으세요.
- 연하곤란(삼킴 장애) — 가장 대표적 증상으로, 처음에는 고형식만 걸리다가 점차 유동식·물까지 삼키기 어려워집니다.
- 연하통(삼킬 때 통증) — 음식물이 식도를 지날 때 가슴 뒤쪽으로 타는 듯한 통증이 느껴집니다.
- 체중 감소 — 식사량 감소와 종양의 대사 소모로 3~6개월 내 체중이 10% 이상 빠지는 경우가 흔합니다.
- 가슴 뒤 통증·압박감 — 흉골 뒤쪽으로 둔한 통증이 지속되며, 심장 질환으로 오인되기도 합니다.
- 만성 기침·쉰 목소리 — 종양이 기관지나 되돌이후두신경을 침범하면 마른 기침·애성(쉰 목소리)이 나타납니다.
- 역류·구토 — 종양으로 식도가 좁아지면 음식물이 역류하고, 심할 경우 음식물 구토가 발생합니다.
- 흑색 변(타르변)·토혈 — 드물지만 종양 표면 출혈로 흑색 변이나 피 섞인 구토가 나타날 수 있습니다.
식도암 원인과 위험인자
식도암의 발생에는 여러 환경적·생활습관적 요인이 복합적으로 작용합니다. 조직학적 유형(편평세포암 vs 선암)에 따라 주요 위험인자가 다릅니다.
편평세포암의 주요 위험인자
- 흡연 — 흡연자는 비흡연자 대비 식도 편평세포암 위험이 3~5배 증가합니다.
- 과도한 음주 — 특히 독한 술(소주·증류주)을 자주 마시면 위험이 5~7배까지 높아집니다.
- 흡연 + 음주 복합 — 두 요인이 합쳐지면 위험이 최대 30배까지 상승하는 강력한 시너지 효과가 있습니다.
- 뜨거운 음식·음료 — 65°C 이상의 뜨거운 차·국물을 자주 마시면 식도 점막 손상이 반복되어 암 위험이 증가합니다. WHO/IARC에서 2A군 발암 요인으로 분류합니다.
- 영양 결핍 — 비타민 A, C, E, 셀레늄 등의 결핍이 위험을 높입니다.
선암의 주요 위험인자
- 역류성 식도염(GERD) — 만성 위산 역류가 식도 하부 점막을 손상시킵니다. 역류성 식도염 완벽 가이드에서 자세한 내용을 확인하세요.
- 바렛식도(Barrett’s Esophagus) — GERD로 인해 식도 하부 편평상피가 원주상피로 변한 전암 병변으로, 선암 발생 위험이 30~60배 높습니다.
- 비만 — BMI 30 이상인 경우 복압 상승 → 위산 역류 → 바렛식도 → 선암 경로로 위험이 증가합니다.
편평세포암 vs 선암 핵심 비교
| 구분 | 편평세포암(SCC) | 선암(Adenocarcinoma) |
|---|---|---|
| 호발 부위 | 식도 중·상부(흉부 식도) | 식도 하부(위-식도 접합부) |
| 한국 비율 | 약 90% | 약 8~10% |
| 주요 위험인자 | 흡연, 음주, 뜨거운 음식 | GERD, 바렛식도, 비만 |
| 성별 비율(남:여) | 약 8:1 | 약 7:1 |
| 전암 병변 | 이형성증(dysplasia) | 바렛식도(Barrett’s) |
| 5년 생존율(전체) | 약 15~20% | 약 20~25% |
| 발생 추세(한국) | 감소 추세 | 소폭 증가 추세 |
식도암 진단 검사
식도암이 의심되면 다음 검사들을 단계적으로 시행합니다.
1차 검사: 상부위장관 내시경(위내시경)
식도암 진단의 골드 스탠다드입니다. 내시경으로 식도 점막을 직접 관찰하면서 의심 부위의 조직 생검(biopsy)을 동시에 시행합니다. 루골(Lugol) 용액 염색 내시경은 편평세포 이형성증의 조기 발견에 효과적이며, NBI(Narrow Band Imaging) 등 특수 영상 기술로 미세 병변도 감지할 수 있습니다.
2차 검사: 영상 검사
- 흉부·복부 CT — 종양 크기, 주변 장기 침범, 림프절 전이 여부 확인
- PET-CT — 원격 전이(폐·간·뼈 등) 여부를 평가하는 핵심 검사
- 내시경 초음파(EUS) — 종양의 식도벽 침범 깊이(T병기)와 주변 림프절 상태를 정밀 평가
- 바륨 식도 조영술 — 식도의 협착 정도와 위치를 파악하는 보조 검사
3차 검사: 병기 결정
위 검사 결과를 종합하여 TNM 병기(AJCC 8th edition)를 결정합니다.
- T(종양) — T1(점막·점막하층) → T2(고유근층) → T3(외막 침범) → T4(주변 구조물 침범)
- N(림프절) — N0(전이 없음) → N1(1~2개) → N2(3~6개) → N3(7개 이상)
- M(원격 전이) — M0(없음) → M1(원격 전이 있음)
식도암 병기별 치료법
식도암 치료는 병기, 조직학적 유형, 종양 위치, 환자 전신 상태를 종합적으로 고려하여 다학제 팀(외과·종양내과·방사선종양학과·소화기내과)이 결정합니다.
병기별 표준 치료 전략 비교
| 병기 | 주요 치료법 | 보조 치료 | 5년 생존율(2026 기준) |
|---|---|---|---|
| 0기(Tis) | 내시경 점막하 박리술(ESD) | 추적 내시경 감시 | 90% 이상 |
| 1기(T1) | ESD 또는 식도절제술 | 림프절 침범 시 항암 고려 | 70~85% |
| 2기(T2-T3, N0-N1) | 수술 전 항암방사선(neo-CRT) → 식도절제술 | 수술 후 면역항암제(니볼무맙) 유지 | 35~50% |
| 3기(T3-T4a, N1-N2) | neo-CRT → 식도절제술 | 수술 후 니볼무맙 1년 유지 | 20~35% |
| 4A기(T4b 또는 N3) | 근치적 항암방사선치료(dCRT) | 면역항암제 병용(펨브롤리주맙·니볼무맙) | 10~20% |
| 4B기(M1) | 전신 항암(FOLFOX/CF) + 면역항암제 | 완화 방사선, 스텐트 삽입 | 5% 미만 |
수술: 식도절제술(Esophagectomy)
근치적 수술은 종양이 포함된 식도 일부 또는 대부분을 절제하고, 위(또는 대장·소장)를 끌어올려 재건(reconstruction)하는 대수술입니다.
- 최소침습 식도절제술(MIE) — 흉강경·복강경을 이용해 개흉 없이 시행하며, 출혈·합병증이 적고 회복이 빠릅니다. 2026년 현재 국내 주요 암센터에서 표준 접근법으로 채택하고 있습니다.
- 로봇 보조 식도절제술(RAMIE) — 로봇 팔을 이용해 정밀 림프절 곽청이 가능하며, 최근 대규모 임상에서 MIE 대비 동등하거나 우월한 단기 성적을 보여줍니다.
항암화학요법
식도암에서 사용되는 주요 항암 레지멘:
- CF(시스플라틴 + 5-FU) — 전통적 1차 표준 레지멘
- FOLFOX(옥살리플라틴 + 5-FU + 류코보린) — CF 대비 부작용이 적어 선호도 증가
- 도세탁셀 + 시스플라틴 + 5-FU(DCF) — 고위험 환자에서 사용
- 파클리탁셀 + 카보플라틴 — 고령자·전신 상태 저하 환자에서 고려
면역항암제(Immunotherapy)
2026년 현재 식도암 치료의 가장 큰 변화는 면역관문억제제(Immune Checkpoint Inhibitor)의 도입입니다.
- 니볼무맙(Nivolumab, 옵디보) — CheckMate 577 연구 결과, 수술 전 항암방사선 후 수술한 환자에서 보조 니볼무맙 1년 투여가 무병생존기간(DFS)을 2배 이상 연장함이 확인되어 2기 이상 표준 치료에 포함됩니다.
- 펨브롤리주맙(Pembrolizumab, 키트루다) — KEYNOTE-590 연구에서 진행성·전이성 식도암의 1차 항암 + 펨브롤리주맙 병용이 전체생존기간(OS)을 유의하게 개선했습니다.
- PD-L1 발현 검사 — CPS(Combined Positive Score) 10 이상인 경우 면역항암제 반응률이 높아 치료 전 반드시 확인합니다.
방사선 치료
식도암에서 방사선 치료는 단독 또는 항암제와 병용(항암방사선병합, CRT)으로 시행됩니다.
- 근치적 항암방사선치료(dCRT) — 수술이 어려운 경부 식도암이나 수술 거부·불가 환자에서 근치 목적으로 시행
- 수술 전 항암방사선(neo-CRT) — CROSS 프로토콜(카보플라틴 + 파클리탁셀 + 41.4Gy 방사선)이 전 세계 표준
- 양성자 치료(Proton Therapy) — 심장·폐 등 주변 장기 피폭을 줄여 부작용을 최소화하는 차세대 방사선 치료로, 국내 일부 센터에서 시행 중입니다.
식도암 5년 생존율 — 병기별 상세
2026년 국가암등록통계 기준 식도암 전체 5년 상대생존율은 약 20.5%입니다. 하지만 조기 발견 시 생존율이 크게 달라집니다.
- 국한(Localized, 1기) — 약 47%
- 국소 진행(Regional, 2~3기) — 약 25%
- 원격 전이(Distant, 4기) — 약 5%
최근 면역항암제 도입 후 진행성 식도암의 중앙생존기간이 기존 10~12개월 → 15~17개월로 개선되고 있으며, 향후 개인맞춤 치료와 바이오마커 기반 선택의 발전으로 추가 개선이 기대됩니다.
식도암 수술 후 식단 관리
식도절제술 후에는 위를 끌어올려 재건하기 때문에 식사 방법의 근본적 변화가 필요합니다.
- 소량 빈식(少量頻食) — 1회 식사량을 줄이고 하루 6~8회로 나누어 먹습니다.
- 천천히 꼭꼭 씹기 — 최소 20~30회 씹어 삼킵니다.
- 식후 바로 눕지 않기 — 식후 최소 30분~1시간 상체를 세운 자세를 유지합니다.
- 고단백 식품 우선 — 달걀, 두부, 살코기, 생선 등으로 수술 후 회복에 필요한 단백질을 충분히 섭취합니다.
- 덤핑 증후군 주의 — 고농도 당류(꿀, 주스, 사탕)를 한꺼번에 먹으면 어지러움·설사·식은땀이 발생할 수 있으므로 단 음식은 분산 섭취합니다.
- 영양 보충제 — 수술 후 비타민 B12, 철분, 칼슘 등의 흡수가 떨어지므로 정기적 혈액 검사와 보충이 필요합니다.
식도암 예방법 — 위험 줄이는 7가지 생활습관
- 금연 — 금연 후 10년 경과 시 식도암 위험이 비흡연자 수준으로 감소합니다.
- 절주 또는 금주 — 하루 알코올 30g(소주 약 3잔) 이상의 음주는 피합니다.
- 적정 체중 유지 — BMI 25 미만을 유지하여 역류성 식도염·바렛식도 위험을 줄입니다.
- 뜨거운 음식 식히기 — 국·차·커피는 65°C 이하로 식혀 마십니다.
- 역류 관리 — GERD 증상이 있으면 적극 치료하고, 바렛식도 진단 시 정기 내시경 추적합니다.
- 채소·과일 충분히 섭취 — 항산화 비타민과 식이섬유가 식도 점막을 보호합니다.
- 정기 검진 — 50세 이상 남성으로 흡연·음주 이력이 있다면 2년마다 위내시경을 권장합니다. 위암 완벽 가이드에서 위내시경 검진 전체 과정을 확인할 수 있습니다.
식도암 위험인자별 위험도 증가 배수
| 위험인자 | 위험도 증가(배) | 관련 유형 | 근거 |
|---|---|---|---|
| 흡연(20갑년 이상) | 3~5배 | 편평세포암 | 메타분석(2023) |
| 과도한 음주(매일 50g+) | 5~7배 | 편평세포암 | IARC Monograph |
| 흡연 + 음주 복합 | 최대 30배 | 편평세포암 | 일본 JPHC 코호트 |
| 바렛식도 | 30~60배 | 선암 | 미국 ACG 가이드라인 |
| 비만(BMI ≥30) | 2~4배 | 선암 | 유럽 EPIC 연구 |
| 뜨거운 음료(65°C+) | 1.5~2배 | 편평세포암 | WHO/IARC 2A군 |
| 아칼라시아(식도이완불능증) | 10~30배 | 편평세포암 | 장기 추적 연구 |
자주 묻는 질문(FAQ)
Q1. 식도암 초기에는 정말 증상이 없나요?
네, 식도암 초기(0~1기)에는 식도 내강이 충분히 넓어 삼킴에 문제가 없으므로 자각 증상이 거의 없습니다. 식도 내경의 2/3 이상이 좁아져야 연하곤란이 나타나기 때문에, 증상이 나타났을 때는 이미 진행된 경우가 많습니다. 50세 이상 흡연·음주 이력이 있는 고위험군은 증상 유무와 관계없이 정기 위내시경 검진을 받는 것이 중요합니다.
Q2. 역류성 식도염이 있으면 식도암 위험이 높은가요?
만성 GERD 자체가 직접 암을 일으키는 것은 아니지만, 장기간 위산 역류로 인해 식도 하부 점막이 바렛식도로 변할 수 있으며, 바렛식도는 식도 선암의 전암 병변입니다. GERD 증상이 5년 이상 지속되거나 바렛식도로 진단받았다면 1~3년 주기 추적 내시경을 받아야 합니다. 자세한 내용은 역류성 식도염 완벽 가이드를 참고하세요.
Q3. 식도암 수술 후 정상 식사가 가능한가요?
식도절제술 후에는 위를 끌어올려 재건하므로 위 용량이 줄어들고 식도-위 접합부 기능이 달라집니다. 수술 직후에는 유동식부터 시작하여 3~6개월에 걸쳐 점차 일반식으로 전환합니다. 완전히 정상적인 식사는 어렵지만, 대부분 환자가 소량 빈식 패턴에 적응하여 일상생활에 큰 지장 없이 식사를 유지합니다. 영양사 상담을 통한 개인 맞춤 식단이 중요합니다.
Q4. 면역항암제가 모든 식도암 환자에게 효과가 있나요?
아닙니다. 면역항암제(니볼무맙, 펨브롤리주맙)의 효과는 PD-L1 발현 수준과 밀접합니다. PD-L1 CPS 10 이상인 환자에서 반응률이 높고, CPS 1 미만인 경우 효과가 제한적일 수 있습니다. 또한 MSI-H(고빈도 현미부수체 불안정성) 종양에서도 면역항암제 반응이 좋습니다. 치료 전 PD-L1 검사와 MSI 검사를 통해 적합 여부를 판단합니다.
Q5. 식도암 가족력이 있으면 검진을 더 일찍 받아야 하나요?
식도암은 유방암·대장암만큼 뚜렷한 유전적 소인이 밝혀지지 않았지만, 직계가족(부모·형제) 중 식도암 환자가 있으면 발생 위험이 약 1.5~2배 높다는 연구가 있습니다. 가족력이 있는 경우 40대부터 위내시경을 시작하고, 흡연·음주를 피하며, 역류 증상이 있으면 적극 치료하는 것이 좋습니다.
Q6. 식도암과 위암은 어떻게 다른가요?
식도암과 위암은 발생 부위, 위험인자, 치료 전략이 다릅니다. 식도암은 흡연·음주·역류가 주요 원인이고, 위암은 헬리코박터 파일로리 감염·짠 음식이 주원인입니다. 다만 위-식도 접합부(GEJ) 암은 두 암의 경계에서 발생하여 분류가 복잡하며, 2026년 현재 Siewert 분류법에 따라 치료 전략을 결정합니다. 위암 완벽 가이드도 함께 읽어보시면 차이점을 이해하는 데 도움이 됩니다.
Q7. 식도 스텐트 삽입은 어떤 경우에 하나요?
식도 스텐트(self-expanding metal stent)는 주로 수술이 불가능한 진행성·전이성 식도암에서 식도 폐색으로 인한 삼킴 장애를 완화하기 위해 삽입합니다. 근치 치료가 아닌 완화(palliative) 목적이며, 항암·방사선 치료와 병행할 수 있습니다. 시술은 내시경 유도 하에 10~15분 내에 완료되며, 삽입 후 유동식·연식부터 시작합니다.
Q8. 식도암 치료 후 재발률은 어느 정도인가요?
식도암은 치료 후 2년 이내 재발률이 가장 높아 전체의 약 60~70%가 이 시기에 재발합니다. 주로 림프절·폐·간·뼈로 재발하며, 수술 후 5년까지 정기 추적(3~6개월 간격 CT·내시경)이 필수입니다. 면역항암제 보조 치료(CheckMate 577 프로토콜) 적용 후 재발률이 유의하게 감소하고 있습니다.
마무리 — 식도암, 조기 발견이 생존율을 바꿉니다
식도암은 초기 증상이 미약하여 발견이 늦어지기 쉽지만, 정기 위내시경으로 조기 발견하면 5년 생존율이 70~85%까지 높아집니다. 2026년 현재 면역항암제의 도입으로 진행성 식도암의 치료 성적도 크게 개선되고 있습니다. 흡연·과도한 음주를 피하고, 역류성 식도염을 적극 관리하며, 50세 이상 고위험군은 정기 검진을 받는 것이 가장 확실한 예방법입니다.